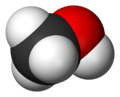
メタノール
| メタノール | |
|---|---|
 |  |
 |  |
IUPAC名 methanol | |
別称 木精 メチルアルコール カルビノール ヒドロキシメタン | |
| 識別情報 | |
CAS登録番号 | 67-56-1 |
PubChem | 887 |
ChemSpider | 864 |
日化辞番号 | J2.364G |
RTECS番号 | PC1400000 |
SMILES
| |
| 特性 | |
化学式 | CH4O |
モル質量 | 32.04 g mol−1 |
示性式 | CH3OH |
| 外観 | 無色液体 |
密度 | 0.7918 g cm-3 |
融点 | -97 °C, 176 K, -143 °F |
沸点 | 64.7 °C, 338 K, 148 °F |
水への溶解度 | 任意に混和 |
蒸気圧 | 133 hPa |
酸解離定数 pKa | ~ 15.5 |
屈折率 (nD) | 1.3292 (20 ℃) |
粘度 | 0.59 mPa·s (20 °C) |
双極子モーメント | 1.69 D(気体) |
| 危険性 | |
EU分類 | |
NFPA 704 |  3 3 0 |
Rフレーズ | R11, R23/24/25, R39/23/24/25 |
Sフレーズ | (S1/2) S7 S16 S36/37 S45 |
引火点 | 11-12 °C |
| 関連する物質 | |
| 関連するアルコール | エタノール プロパノール ブタノール |
| 関連物質 | クロロメタン メトキシメタン |
| 出典 | |
[1]ICSC番号:0057 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
メタノール (methanol) は有機溶媒などとして用いられるアルコールの一種である。別名として、メチルアルコール (methyl alcohol)、木精 (wood spirit)、カルビノール (carbinol)、メチールとも呼ばれる。一連のアルコールの中で最も単純な分子構造を持つ。ホルマリンの原料、アルコールランプなどの燃料として広く使われる。燃料電池の水素の供給源としても注目されている。
目次
1 製法
2 主要な用途
3 主な化学反応
4 危険性
4.1 引火
4.2 飲用毒性
4.3 各国の中毒における事例
4.3.1 日本
4.3.2 イタリア
4.3.3 ケニア
4.3.4 中国
4.3.5 韓国
4.3.6 ベトナム
4.3.7 インドネシア
4.3.8 ウガンダ
4.3.9 インド
4.3.10 リビア
4.3.11 ロシア
5 出典
6 関連項目
製法
木材由来による木酢液の蒸留("木精"という名の由来)。
石炭ないし天然ガスの部分酸化で製造した一酸化炭素 (CO) に、酸化銅-酸化亜鉛/アルミナ複合酸化物を触媒として、50-100気圧、240-260℃で水素 (H2) を反応させる[2]。
- CO+2H2⟶CH3OH{displaystyle {ce {CO + 2H2 -> CH3OH}}}
- CO+2H2⟶CH3OH{displaystyle {ce {CO + 2H2 -> CH3OH}}}
- メタノール産生菌による発酵。
現代の工業製法はコスト面の事情により2.の製法で天然ガスからの製造が主流である。
主要な用途
化学用途 フェノール樹脂や接着剤、酢酸およびホルマリンの合成原料。さまざまな化学反応の溶媒のため、中間製品として多様な産業で用いられる。
燃料用途 石油代替自動車燃料としてはエタノールより安価でCNGと並ぶ価格競争力がある(詳細:アルコール燃料)。また、ノートパソコンなどのモバイル機器を長時間稼動させるため、直接メタノール燃料電池 (DMFC) が期待されている。
主な化学反応
- 燃焼時の反応で二酸化炭素と水が生成する。
- 2CH3OH+3O2⟶2CO2+4H2O{displaystyle {ce {2CH3OH + 3O2 -> 2CO2 + 4H2O}}}
- 2CH3OH+3O2⟶2CO2+4H2O{displaystyle {ce {2CH3OH + 3O2 -> 2CO2 + 4H2O}}}
- 熱した銅 (Cu) と反応して酸化するとホルムアルデヒド (HCHO) が生成する。
- CH3OH+CuO⟶HCHO+Cu+H2O{displaystyle {ce {CH3OH + CuO -> HCHO + Cu + H2O}}}
- CH3OH+CuO⟶HCHO+Cu+H2O{displaystyle {ce {CH3OH + CuO -> HCHO + Cu + H2O}}}
ナトリウム (Na) と反応して、ナトリウムメトキシド (CH3ONa) と水素 (H2) が生成する。
- 2CH3OH+2Na⟶2CH3ONa+H2{displaystyle {ce {2CH3OH + 2Na -> 2CH3ONa + H2}}}
- 2CH3OH+2Na⟶2CH3ONa+H2{displaystyle {ce {2CH3OH + 2Na -> 2CH3ONa + H2}}}
危険性
引火
日本においてメタノールは危険物第四類アルコール類に指定されているなど、引火の危険性の高い液体である。揮発性が高く、メタノールの入った容器を直接火にかけると爆発する恐れがあるため、保管場所・使用場所における火気や電気火花について念入りに注意しなければならない。特に使用する場所では十分な換気と、容器を倒さないこと、液をこぼさないことに留意されたい。換気は防火上有効であるとともに、後述する中毒の防止にも有効である。
一般的な油火災(B火災)同様に引火して炎上した際は、粉末の消火器、二酸化炭素、砂を用いる。噴霧注水は差し支えないが、注水消火は、薄められたメタノールが溢れ火災が広がる可能性があり、極少量の火災以外には用いない。泡消火は泡がメタノールに吸収されてしまうので、泡消火薬剤を用いる場合は特に耐アルコール性の泡消火薬剤を用いる。
メタノールの炎は薄青色であるが、特に昼間は視認しにくい。キャンプ用品として販売されている木炭用の着火剤はゲル状物質にメタノールが含まれている。特に復元性を持つ樹脂容器に充填された製品は着火後に継ぎ足すと、容器内の空洞に生じた可燃性混合気に引火・破裂拡散し火のついたゲル状燃料を撒き散らす危険があるので決して着火後に継ぎ足してはならない。この種の事故が相次いだ為に使いかけの製品でも容器内に空洞を生じない製品も多い。金属製チューブ・使い切りのパック入りの製品ではこの危険は無い。また、適正な使用であっても、炎が見難いために火傷を負う事故がある。
飲用毒性
メタノール毒性も参照
メタノール中毒は、取り扱い時の吸入、故意の摂取、誤飲などで起こる。メタノールの致死量に関しては様々な報告があり、個人差が大きいと考えられるが、ヒト、経口での最小致死量は0.3-1.0g/kg程度であると考えられている。これはエタノールの1/10程度の量である。ヒトを含む霊長類の場合、メタノールはアルコールデヒドロゲナーゼによってホルムアルデヒドに代謝され、さらにホルムアルデヒドデヒドロゲナーゼによってギ酸に代謝される。ホルムアルデヒドの体内半減期はおよそ一分であり、ホルムアルデヒドからギ酸への代謝は迅速に行われるため、ホルムアルデヒドによる毒性はほとんど問題にならない[3]。メタノールの毒性はギ酸による代謝性アシドーシスとニューロンへの毒性によるものである。ギ酸の代謝能力は種によって異なっており、げっ歯類に比べてギ酸の代謝能力に劣る霊長類はメタノールの毒性が強く出ることが知られている[3]。
メタノール中毒による症状としては、目の網膜を損傷することによる失明がよく知られている。これは次の網膜でのメカニズムによる。βカロテンが鎖の真ん中で切断されると2分子のトランス型のレチノールというアルコール型のビタミンAを生成する。このレチノールは酸化されてレチナールというアルデヒドになるが、このトランス型のレチナールはシス型のレチナールに変化してオプシンというタンパク質に収納される。このレチナールとオプシンの複合体がロドプシンである。ロドプシンに光が当たり、シス型だったレチナールが安定なトランス型に戻ると、レチナール分子はオプシンに収まらず外れてしまう。この変化が細胞内を伝わり化学的に増幅され、「光が当たった」という信号となって視神経に伝播する。トランス型レチナールは再びイソメラーゼの働きでシス型に折り曲げられてオプシンに収納されるが、やがてレチナールは消耗し不足してゆく。そして、この不足した分はレチノールから酸化して補われる。網膜にはレチノールをレチナールに酸化するためのアルコール脱水素酵素が豊富に存在するため、メタノールを飲んだ場合には網膜でホルムアルデヒドが大量に作られ、そのホルムアルデヒドの毒性が視細胞に悪影響を及ぼし、その結果として失明することになる[4]。ホルムアルデヒドは短時間でギ酸に代謝される(上記参照)。ギ酸は、10-ホルミルテトラヒドロ葉酸合成酵素によりテトラヒドロ葉酸から10-ホルミルテトラヒドロ葉酸を経て代謝、分解される。ヒトではこの反応速度が遅いためギ酸が残留して毒性を示すこととなる。メタノール中毒による視力障害は、ギ酸の直接傷害による視神経の脱髄が原因と考えられるが、軸索の損傷も示唆する報告がある[5]。またギ酸がミトコンドリアの電子伝達系に関わるシトクロムオキシダーゼを阻害するために視神経毒性が現れるとする意見もある[3]。
メタノールとギ酸はともに血液透析により効率よく除去することができる。また、生体内でのギ酸分解を促進するために活性型葉酸の投与が推奨される[5]。
日本ではエタノールを混合していないメタノールは劇物であり、購入時の毒劇物譲受書への署名捺印を義務付けられている。
各国の中毒における事例
日本
戦前の1933年にメタノールで増嵩ししたカストリの飲用から30名以上の死者が出たほか、第二次世界大戦後の混乱期には安価な変性アルコールを用いた密造酒によるメタノール中毒もしばしば起きた。
エタノールは酒税の課税対象となるが、エタノールにメタノールなどを加えた変性アルコールは非課税であり、これらは安価であった。このエタノールにメタノールが混入された変性アルコールを蒸留して、すなわち、"メタノールとエタノールの沸点は異なるので、適切な温度で蒸留したら分離できるだろう"という目論見で、変性アルコールを加熱・蒸留してエタノールを分離しようとしたものを密造酒として供することが横行した。しかし、メタノール-エタノール混合溶液は共沸混合物であり、メタノールとエタノールの沸点が異なっていても、混合溶液となったものを単純に加熱してメタノールを取り除くことは不可能で(共沸)、この結果、メタノールを除去できていない変性アルコールがカストリ酒となって広く出回り、中毒事故が多発した。
失明者が多く出たことから、メタノールの別称である「メチルアルコール」を当てて「目散るアルコール」や、その危険性を象徴してバクダン等と呼ばれた。
イタリア
1986年、メタノール入りのワインを飲んで22人が死亡した[6]。
ケニア
ケニアで一般的に飲まれているトウモロコシの発酵酒は、製造時にメタノールを添加し、アルコール度数を高める手法が密かに行われている。その添加量は中毒患者が出るギリギリで調節されているというが、しばしば中毒事件が発生する。2000年には、「チャンガー」と呼ばれる密造酒により134人が死亡、1000人以上が病院に収容される大事件が発生したほか、2005年にも30人程度の死亡者が発生するなど事件は後を絶たない。
中国
1998年の旧正月直前に、山西省でメタノールが入った密造酒による中毒死事件が起きた。約400人が入院し、約30人が死亡した。
韓国
1988年のソウルオリンピックの際にソ連のオリンピック協会職員が、薬局でエタノールを購入しようとしたところ(当時のソ連の財政難とルーブルの暴落のために、通常の酒類が購入できなかった)誤ってメタノールを購入してこれを飲んでしまい、死亡する事故が起こった。
ベトナム
零細な酒造メーカーにおいては、蒸留酒のアルコール度数を増やすために、安価な燃料用メタノールを混入することが常習的に行われていることがある。2008年にもホーチミン市において20人程度の死亡者が出た。
インドネシア
2009年5月、バリ島でメタノールが混じった酒を飲んで中毒を起こす人が続出。外国人を含む20人以上が死亡、多数が入院する事態となった。地元の酒造業者がアラック(米やヤシの実が原料の蒸留酒)にメタノールを混ぜて製造した酒が原因とみられる。
ウガンダ
2010年4月、ウガンダの南西のカバレ県、カムウェンゲ県において、メタノールが混入したワラギ(東アフリカの蒸留酒)による多臓器不全が原因となり、3週間で89人が死亡、100人以上が入院するという事件が起きた[7](英語版ワラギの項目も参照)。
インド
2011年12月、インド西ベンガル州で違法に醸造されたメタノール入りの酒を飲んだ労働者がメタノール中毒を起こし、140人以上の死者、100人以上の入院患者を出した[8]。
リビア
2013年3月、首都のトリポリにてメタノール入りの密造酒による中毒が原因で50人以上が死亡、400人近くが病院で手当を受けた[9]。
ロシア
2014年3月、東シベリア・ザバイカル地方の村で、住民らがメタノール入りのウォッカを飲んだ後に、14人が死亡、12人が重症となった。
2016年12月、ロシア・シベリア地方のイルクーツクで、人体に有害なメタノール入りの入浴剤を安い酒代わりに飲んだ住民49人が死亡した[10]。背景には、2010年からウォッカの最低小売価格が2倍になったことにあり、ロシア国内で年間1万3,000人以上が死亡していると見られている[11]。
出典
^ “The Emergency Response Safety and Health Database: Systematic Agent: METHANOL”. Centers for Disease Control and Prevention. 2009年8月26日閲覧。
^ K. Weissermel, H.-J. Arpe 『工業有機化学 第5版』 東京化学同人、2004年。ISBN 978-4807906055。
- ^ abcICPS INCHEM. “ENVIRONMENTAL HEALTH CRITERIA 196 Methanol”. 2014年5月9日閲覧。
^ 「続・身のまわりの毒」Anthony T.Tu著、東京化学同人、1993年
- ^ abTop of the basilar syndromeを疑われたメタノール中毒の1症例、佐々木庸郎 ほか、日本救急医学会雑誌 Vol.19 (2008) No.3 P160-167
^ 大阪府立公衆衛生研究所メールマガジン かわら版@iph -第71号- 2009年7月31日発行
^ "When African brewers ferment death", Daily Monitor, April 25 2010.
^ 密造酒飲み143人死亡、100人以上が入院 インド・西ベンガル州(AFP.BB.NEWS 2011年12月16日)同日閲覧
^ リビア、密造酒飲んで数百人が中毒に 50人以上死亡 AFP 2013年3月12日
^ 入浴剤飲み49人死亡、ロシア都市が非常事態宣言 AFP=時事 2016年12月20日
^ ロシア、ウォッカ値上げで代替の入浴剤飲み年1.3万人死亡 NEWSポストセブン(2017年4月22日)2017年4月23日閲覧
関連項目
- エタノール
アルコール(化学)- アルコール燃料
- 直接メタノール燃料電池
- 化学性食中毒
| ||||||||||



